Typologie d'actualités : GT Signalisation cellulaire et neurofibromatose
Collaboration avec Béatrice Vallée, co-responsable de l’équipe Signalisation cellulaire et Neurofibromatose

Bojan Žunar est assistant professeur à l’Université de Zagreb, Faculté de technologie agro-alimentaire et de biotechnologie dans le département de biochimie. Il vient pour 2 mois dans l’équipe Signalisation cellulaire et Neurofibromatose.
Bojan n’est pas un inconnu au CBM puisqu’il a effectué un stage post-doctoral dans la même équipe en 2020-2021.
Maintenant, il dirige sa propre équipe, et il a été lauréat d’un financement européen (https://croestro.eu/, NextGenerationUE) lui permettant, lui et plusieurs de ses étudiants, de venir au CBM réaliser des expériences et profiter des équipements d’imagerie de la plateforme Mo2Ving.
Ses domaines de recherche concernant la biologie synthétique et l’édition génétique de la levure afin de développer des biocapteurs humanisés et des cellules usines microbiennes innovantes dans les domaines de la recherche fondamentale mais aussi appliquée notamment en environnement et pour l’industrie.
nouvelle stratégie thérapeutique anti-cancer ciblant les protéines kinases LIMKs via le développement de molécules innovantes
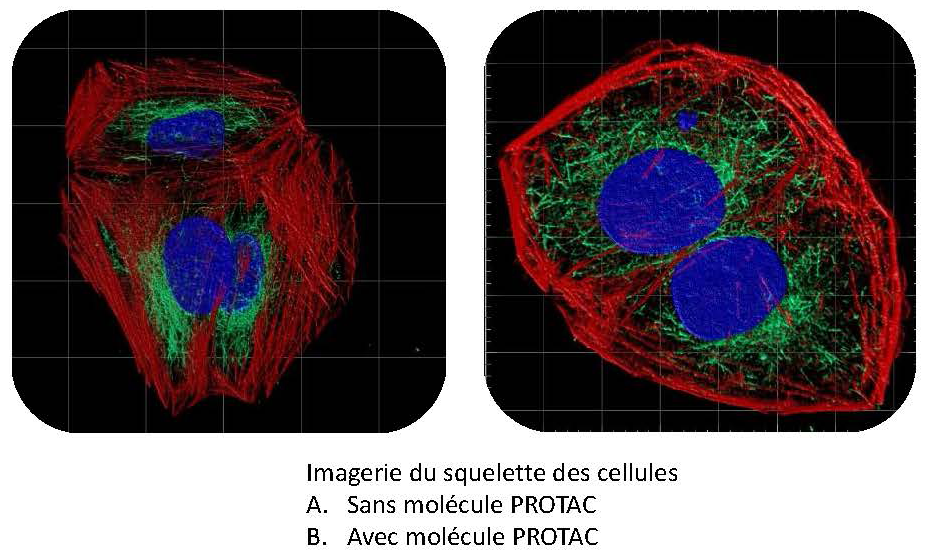
Des avancées significatives ont été réalisées ces dernières années en oncologie avec une augmentation de l’espérance de vie et une morbidité moindre pour les patients traités. Cependant, certains cancers ont toujours un pronostic sombre et de nombreuses résistances aux traitements classiques sont observées. Il est donc primordial de continuer à développer de nouvelles thérapies.
Les protéines kinases LIMKs sont surproduites dans de nombreux cancers et constituent donc des cibles thérapeutiques d’intérêt. Des petites molécules chimiques ciblant l’activité kinase des LIMKs ont été développées ces 15 dernières années mais aucune n’est arrivée au stade des essais cliniques. En collaboration avec des chimistes de l’ICOA, Karen Plé et Sylvain Routier, nous développons une nouvelle catégorie de petites molécules chimiques innovantes, des PROTACs, qui visent à limiter voire éteindre totalement la production de ces protéines LIMKs. Les premiers résultats obtenus sont très prometteurs, puisque deux des molécules synthétisées par les chimistes éteignent totalement la production des LIMKs et des effets drastiques sur cellules sont observés. Il nous faut désormais caractériser plus avant ces molécules et décortiquer leurs effets cellulaires pour ouvrir la voie vers une nouvelle stratégie thérapeutique efficace ciblant les LIMKs.
La Fête de la Science au CBM : un franc succès !
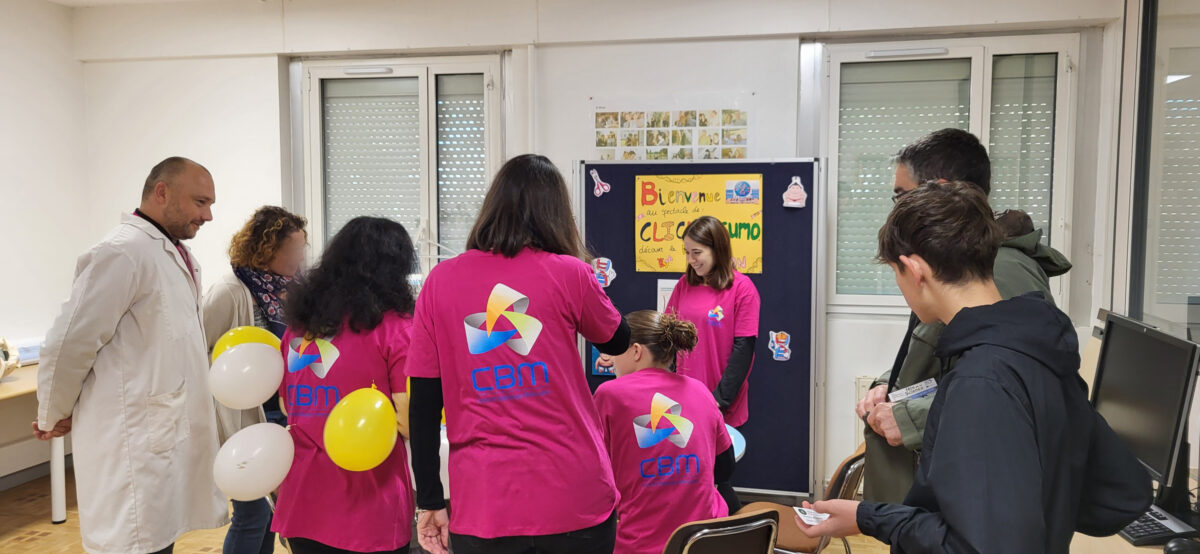
Vincent James, animateur de la radio France Bleu Orléans, à rencontré 3 chercheurs sur le campus CNRS d'Orléans. Il a interviewé Béatrice Vallée, biologiste de l'équipe "Signalisation cellulaire et neurofibromatose", qui a présenté ses travaux sur les biocapteurs à base de levure et sa participation à la Fête de la Science.
A écouter en podcast (émission du 4 octobre, interview de Béatrice Vallée à 6mn30).
Les visiteurs, de tous âges, ont été très contents de pouvoir rencontrer des scientifiques et participer à différents ateliers.
Conférence « Le traitement de l’eau à l’échelle microscopique, découvrez les recherches en cours »

Cette conférence à trois voix vous plonge dans l’eau à une échelle microscopique. Trois chercheurs du CNRS Béatrice Vallée, biologiste et co-responsable de l'équipe "Signalisation cellulaire et neurofibromatose", Cyprien Soulaine , modélisateur du sous-sol à l'ISTO et Pascal Brault, physicien au GREMI, aborderont le thème de l’eau sous 3 angles : la ressource, la pollution et les traitements actuellement disponibles.
Cette conférence est organisée dans le cadre des Echappées Inattendues du CNRS et de la Fête de la Science 2024.
Mardi 8 octobre 2024 à 19 h au Muséum d'Orléans pour la Biodiversité et l'Environnement (MOBE), 6 rue Marcel Proust, 45000 Orléans.
Une maladie génétique : la neurofibromatose – Comprendre pour guérir
Samedi 5 et dimanche 6 octobre de 13 h à 18 h
Visite à partir de 11 ans, durée 30 minutes.
Avec les membres de l'équipe "Signalisation cellulaire et neurofibromatose", venez découvrir comment ils élucident les mécanismes dérégulés dans la maladie pour élaborer des thérapies innovantes.
Lire la présentation de la visite sur le site de la Fête de la Science
La professeure Anna Wawruszak, de l’Université de médecine de Lublin, chercheure invitée LE STUDIUM est reçue au CBM de septembre à novembre 2024

Biographie
Diplômée de l'université Maria Curie-Sklodowska en biotechnologie médicale et en chimie des agents bioactifs et des cosmétiques (études de maîtrise) respectivement en 2013 et 2014, elle a obtenu son doctorat au département de biochimie et de biologie moléculaire de l'université médicale de Lublin en 2020. Depuis lors, elle travaille à l'université médicale de Lublin en tant que post-doctorante, chercheuse et, enfin, chef de groupe (professeur associé). Son expertise principale porte sur la médecine translationnelle, l'épigénétique et la recherche sur le cancer du sein. Ses travaux sont principalement axés sur l'activité anticancéreuse des inhibiteurs de l'histone désacétylase dans des modèles de cancer du sein. Elle s'intéresse également à la chimie verte et aux approches biotechnologiques pour le développement de produits cosmétiques naturels.
Projet : GreenCosmIn - chimie verte et approches biotechnologiques pour le développement de produits cosmétiques naturels
GreenCosmIn vise à établir un réseau robuste, multisectoriel et interdisciplinaire pour mettre en œuvre des approches respectueuses de l'environnement dans l'exploration et l'exploitation des ressources naturelles, en mettant l'accent sur la production de cosmétiques. Le projet évaluera l'activité biologique d'extraits sélectionnés et/ou de composés isolés en utilisant diverses plateformes, y compris des outils in vitro, avec des kératinocytes et des monocouches de mélanome et des modèles 3D testés dans différentes conditions de concentration d'oxygène (normoxie/hypoxie). Le criblage in vitro d'extraits, de fractions ou de composés isolés/sémisynthétisés sera effectué pour évaluer leur capacité à inhiber des enzymes spécifiques pertinentes pour les applications cosmétiques. Après traitement avec des produits naturels, des paramètres tels que l'activité antioxydante, la peroxydation des lipides, le vieillissement de la peau, la pigmentation, la production de ROS ou l'activité de la catalase SOD, seront déterminés.












