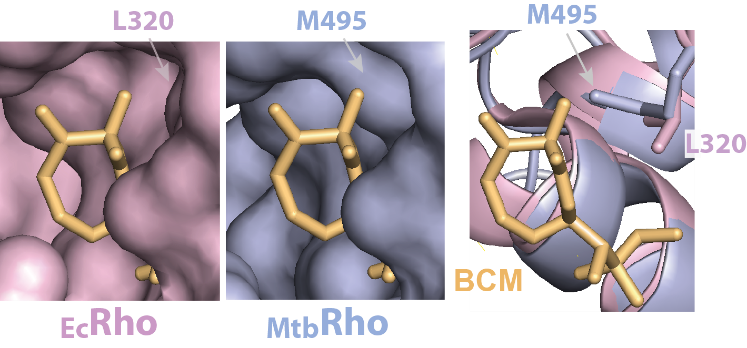
Le facteur bactérien Rho est un moteur moléculaire qui induit la terminaison de la transcription à l'échelle du génome. Rho est essentiel chez de nombreuses espèces, y compris chez Mycobacterium tuberculosis où l'inactivation du gène rho entraîne une mort rapide. Néanmoins, le facteur Rho de M. tuberculosis [MtbRho] présente des idiosyncrasies dont une résistance à l’antibiotique bicyclomycine [BCM], qui restent inexpliquées. Pour identifier l’origine moléculaire de ces spécificités, nous avons résolu la structure de MtbRho par cryo-EM à 3.3 Å. Cette structure atomique révèle notamment une substitution leucine→méthionine qui crée un encombrement stérique dans les sites de liaison de la BCM, près des sites ATPase, conférant ainsi une résistance à la BCM au détriment de l'efficacité de moteur moléculaire. Notre travail contribue à expliquer les propriétés inhabituelles de MtbRho et fournit un cadre précis pour le développement de futurs antibiotiques.
Catégorie d'actualités : Publications marquantes
J.-M. Bonmatin co-auteur d’un article faisant le lien entre insecticides néonicotinoïdes et les maladies rénales chroniques d’étiologie indéterminée (CKDu)
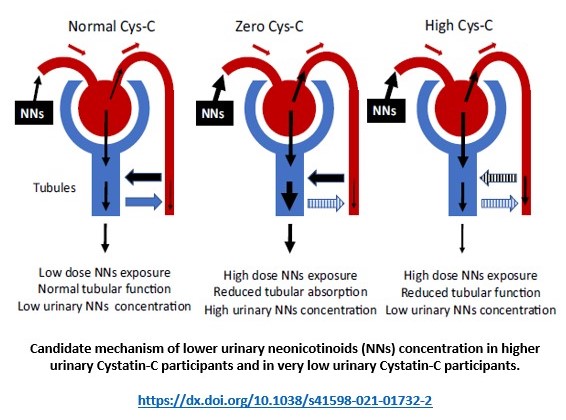
Les maladies rénales chroniques (Chronic Kidney Diseases : CKD) sont un fléau qui fait de plus en plus de victimes dans le monde et en particulier dans les pays moins développés où l’agriculture est intensive. Plusieurs facteurs de risques ont été identifiés, mais il subsiste une étiologie indéterminée (CKDu) pouvant être liée aux pesticides (Floris et al., 2021).
J.-M. Bonmatin a participé à une étude au Sri Lanka et publiée dans Scientific Reports fin 2021 (Taira et al., 2021). Même si la dimension de l’étude reste statistiquement modeste, les auteurs (membres de la Task Force on Systemic Pesticides) ont montré que les concentrations de plusieurs insecticides néonicotinoïdes mesurées dans les urines, étaient en lien avec les biomarqueurs Cystatin-C et L-FABP ainsi qu’avec les symptômes neurophysiologiques observés. Les auteurs concluent que les concentrations urinaires de ces néonicotinoïdes seraient un facteur de risque des troubles tubulaires du rein. C’est un élément de plus qui s’ajoute à nos publications précédentes (ex : Ichikawa et al., 2019 et Bonmatin et al., 2021) sur les effets de ces insecticides sur la santé humaine.
Les néonicotinoïdes dits « tueurs d’abeilles » et qui sont à la source d’impacts majeurs sur la biodiversité (invertébrés et vertébrés) restent encore très largement utilisés pour la culture du riz en Asie (Prihandiani et al., 2021). Ces insecticides sont désormais interdits en France depuis 2018 (sauf pour la betterave sucrière). Ils sont en passe d’être interdits au Sri Lanka.
Référence : Taira K, Kawakami T, Weragoda SK, Herath HMAS, Ikenaka Y, Fujioka K, Hemachandra M, Pallewatta N, Aoyama Y, Ishizuka M, Bonmatin JM & Komori M (2021) Scientific Reports, 11, 22484.
https://doi-org.inc.bib.cnrs.fr/10.1038/s41598-021-01732-2
Les premières molécules qui préfèrent le manganèse(II) au zinc(II)
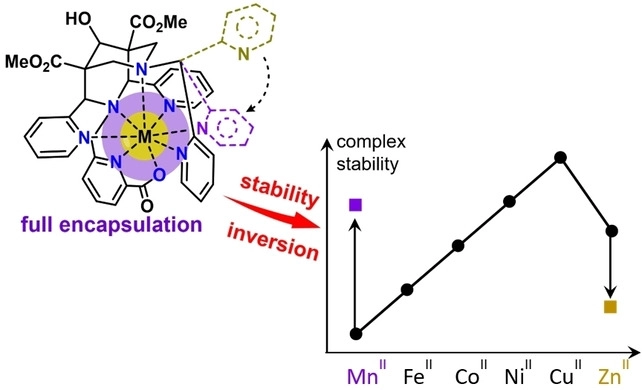
Des complexes de manganèse(II) rencontrent de plus en plus d’intérêt dans les applications biomédicales, surtout en imagerie en tant qu’agents de contraste plus biocompatibles que ceux actuellement utilisés. Néanmoins, le manque de ligands capables de former des complexes très stables et sélectifs vis-à-vis du zinc(II), le compétiteur biologique principal, constitue un verrou important. Dans un article dans l’Angewandte Chemie Int. Ed., le groupe “Complexes métalliques et IRM”, en collaboration avec l’équipe de Peter Comba de l’Université de Heidelberg, a identifié les premières molécules cage qui satisfont ces critères. Ces bispidines possèdent une cavité de coordination très rigide et d’une taille parfaitement adaptée au MnII, permettant ainsi d’obtenir des stabilités record. En revanche, le ZnII forme des complexes peu stables car sa taille est trop petite et ne permet pas d’accommoder toutes les fonctions coordonnantes du ligand. Des calculs théoriques combinés avec des données expérimentales ont démontré une sélectivité inégalée, avec une stabilité jusqu’à dix ordres de grandeur supérieure pour les complexes de manganèse que pour ceux du zinc(II).
https://onlinelibrary.wiley.com/doi/full/10.1002/anie.202115580
Une nouvelle luminescence pour suivre en direct la libération de médicaments
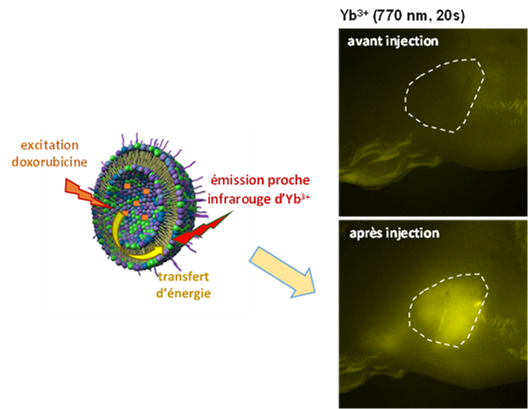
Les liposomes sont des nanocapsules très utilisées pour transporter et libérer des agents thérapeutiques ou diagnostiques, ou les deux, in vivo. L’agent thérapeutique ne devient actif que lors de sa libération, évitant d’endommager les tissus sains. Être capable de suivre en direct cette libération est crucial pour comprendre et contrôler son action.
Les approches d’imagerie optique précédemment proposées utilisent exclusivement des fluorophores organiques ou des nanoparticules inorganiques, co-encapsulés dans le liposome avec le principe actif.
La luminescence des complexes de lanthanides est une alternative qui offre de nombreux avantages, notamment la capacité d’émission dans le domaine proche-infrarouge (NIR), facilitant ainsi la détection dans des systèmes biologiques.
Les équipes du CBM ont mis au point un assemblage innovant : un liposome constitué d’un complexe d’Ytterbium qui contient la molécule anticancéreuse doxorubicine. La luminescence NIR du complexe de lanthanide est observable uniquement en présence du médicament dans le liposome. Ce signal de luminescence NIR devient un outil pour le suivi direct et en temps réel de l’intégrité du liposome et, ainsi, de la libération du médicament.
Cette luminescence provenant du lanthanide a pu être détectée in vivo dans une souris porteuse d’une tumeur mammaire.
Références de l'article :
Doxorubicin-sensitized Luminescence of NIR-emitting Ytterbium Liposomes: Towards Direct Monitoring of Drug Release, Sara Lacerda, Anthony Delalande, Svetlana V. Eliseeva, Agnès Pallier, Célia S. Bonnet, Frédéric Szeremeta, Sandra Même, Chantal Pichon, Stéphane Petoud, Eva Toth, Angewandte Chemie Int. Ed. 13 août 2021 https://doi.org/10.1002/anie.202109408
Voir l'actualité sur le site de l'Institut de Chimie du CNRS
Nouvelle avancée méthodologique en synthèse totale de protéines
Depuis la synthèse du premier dimère d’acide aminé à la fin du 19ème siècle, la synthèse de protéines a constitué un objectif fascinant pour des générations de chimistes. Inventée dans les années 1960, la synthèse peptidique sur support solide est depuis utilisée en routine pour des peptides constitués de quelques dizaines d’acides aminés. La découverte des réactions de « ligation chimique » dans les années 1990 a rendu possible la synthèse de protéines de plus de cents acides aminés : des réactions chimiques extrêmement sélectives sont ici mises en œuvre pour lier des segments peptidiques –eux-mêmes synthétisés par SPPS– et dont les chaines latérales ne sont pas protégées par les groupements protecteurs habituellement utilisés en synthèse organique. Grace à ces avancées méthodologiques, l’approche « chimique » de la synthèse de protéines complète aujourd’hui avantageusement les méthodes biotechnologiques et permet de générer des protéines natives ou modifiées, outils sur-mesure pour décrypter le vivant à une résolution atomique.
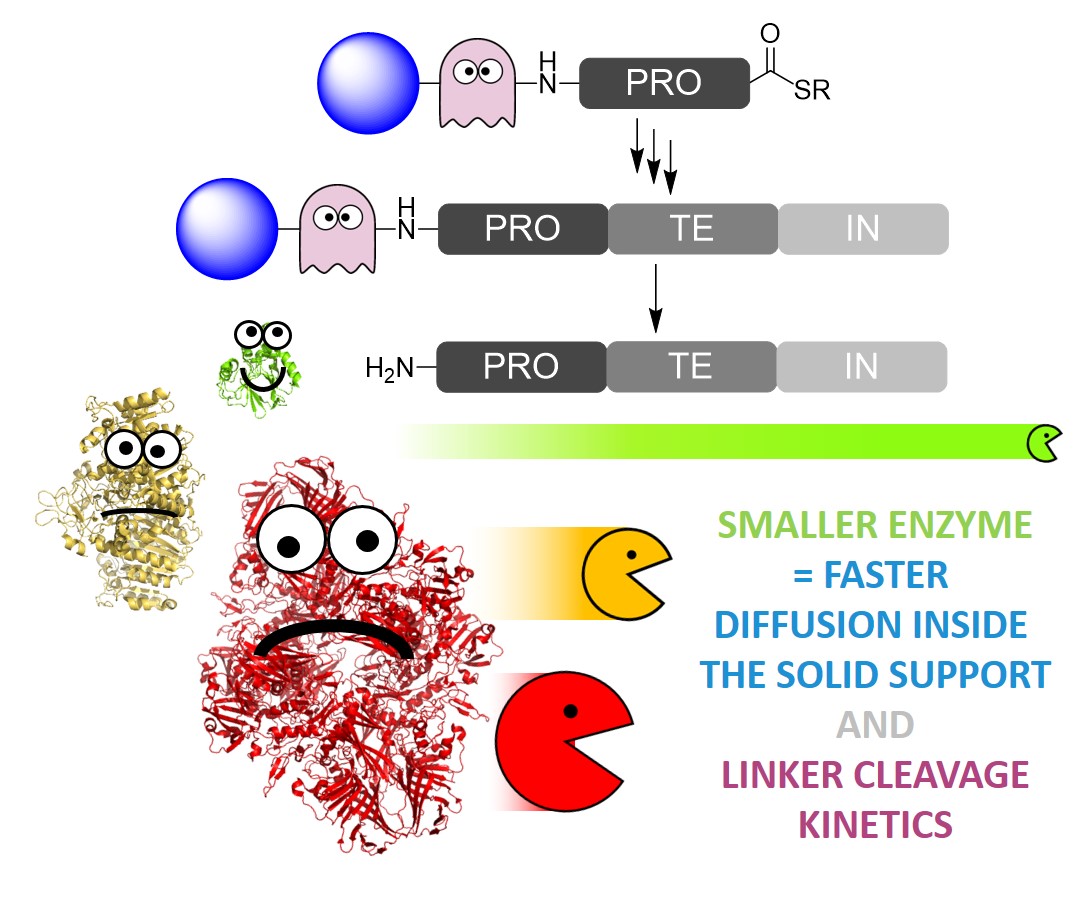
Toutefois, la synthèse de protéines de plusieurs centaines d’acides aminés requiert de nombreuses ligations chimiques successives, et donc des étapes particulièrement délicates de purification des intermédiaires réactionnels. Une solution pour s’affranchir de ces étapes est d’assembler les protéines par ligation sur un support solide. Bien que très attrayante, cette approche a été limitée à des preuves de concept : l'une des raisons principales est la difficulté de greffer sur un support solide adapté le premier segment peptidique via un bras (linker) qui doit pouvoir être coupé facilement une fois les ligations effectuées. En effet, les conditions requises pour la coupure des bras développés jusqu’ici sont incompatibles avec de nombreuses protéines.
Pour pallier ce problème les scientifiques du CBM, en collaboration avec des collègues de l’IC2MP de Poitiers, ont exploré des bras programmés pour être coupés dans des conditions très douce par une réaction enzymatique. De façon remarquable, La taille de l'enzyme est directement corrélée à la vitesse de coupure du bras, et donc à l’efficacité de la libération de la protéine synthétisée. La méthode a été appliqué à la synthèse d'un peptide de 160 acides aminés, qui est à ce jour la plus longue séquence jamais synthétisée par ligations chimiques sur support solide.
Référence de l’article : S. A. Abboud, M. Amoura, J.-B. Madinier, B. Renoux, S. Papot, V. Piller, V. Aucagne. Enzyme-cleavable linkers for protein chemical synthesis through solid-phase ligations, Angew. Chem. Int. Ed., 2021, accepted article. https://doi.org/10.1002/anie.202103768
Voir l'actualité sur le site de l'Institut de Chimie du CNRS
J.-M. Bonmatin co-auteur d’une lettre dans Science (16 juillet 2021)

Un ensemble de co-auteurs spécialistes des pollinisateurs vient de publier une lettre dans Science (Simon-Delso at al. 2021). Cette lettre est un appel aux Ministres européens pour réagir en responsabilité et réduire les risques toxiques pour les pollinisateurs lors des évaluations des pesticides. Par exemple, si la mortalité naturelle des abeilles domestiques peut atteindre jusqu’à 5%, la communauté scientifique s’accorde sur un taux « acceptable » maximum de 7% pour un pesticide. Accepter 10%, c’est prendre un risque bien trop élevé en regard de la situation déjà catastrophique quant à l’effondrement des pollinisateurs. Du fait de l’importance cruciale de telles décisions pour le la planète et notre futur, les auteurs et l’éditeur ont choisi un style plus direct qu’habituellement pour passer leur message.
Référence : Simon-Delso N, Aebi A, Arnold G, Bonmatin JM, Hatjina F, Medrzycki P & Sgolastra F (2021) Maximize EU pollinator protection: Minimize risk, Science, 373(5552), 290. DOI: 10.1126/science.abj8116
Comment l’environnement hydrothermal de la Terre Primitive a pu influencer le choix du sucre constitutif de l’ADN et de l’ARN

Pourquoi le furanose est-il le seul sucre que l’on retrouve dans la composition de l’ADN et l’ARN alors que cette forme de sucre n’est pas la plus stable, donc pas la plus abondante, dans les conditions de température et de pression que nous connaissons actuellement ? Ce sont les sources hydrothermales, omniprésentes à la surface de la Terre primitive, et leur influence thermique complexe, qui pourraient être à l’origine de cette sélectivité. Cette étude menée par les scientifiques du Centre de biophysique moléculaire, qui fait l’objet d’un article dans la revue Nature Communications, devrait permettre de mieux comprendre pourquoi et comment les molécules s’assemblent pour donner la vie dans un contexte géologique primitif.
Référence
Avinash Vicholous Dass, Thomas Georgelin, Frances Westall, Frédéric Foucher, Paolo De Los Rios, Daniel Maria Busiello, Shiling Liand & Francesco Piazza
Equilibrium and non-equilibrium furanose selection in the ribose isomerisation network
Nature Communications, 12 2749 (2021) https://www.nature.com/articles/s41467-021-22818-5